Archive
- Home
- 2024/5
- 2024/4
- 2024/3
- 2024/2
- 2024/1
- 2023/12
- 2023/11
- 2023/10
- 2023/9
- 2023/8
- 2023/7
- 2023/6
- 2023/5
- 2023/4
- 2023/3
- 2023/2
- 2023/1
- 2022/12
- 2022/11
- 2022/10
- 2022/9
- 2022/8
- 2022/7
- 2022/6
- 2022/5
- 2022/4
- 2022/3
- 2022/2
- 2022/1
- 2021/12
- 2021/11
- 2021/10
- 2021/9
- 2021/8
- 2021/7
- 2021/6
- 2021/5
- 2021/4
- 2021/3
- 2021/2
- 2021/1
- 2020/12
- 2020/11
- 2020/10
- 2020/9
- 2020/8
- 2020/7
- 2020/6
- 2020/5
- 2020/4
- 2020/3
- 2020/2
- 2020/1
- 2019/12
- 2019/11
- 2019/10
- 2019/9
- 2019/8
- 2019/7
- 2019/6
- 2019/5
- 2019/4
- 2019/3
- 2019/2
- 2019/1
- 2018/12
- 2018/11
- 2018/10
- 2018/9
- 2018/8
- 2018/7
- 2018/6
- 2018/5
- 2018/4
- 2018/3
- 2018/2
- 2018/1
- 2017/12
- 2017/11
- 2017/10
- 2017/9
- 2017/8
- 2017/7
- 2017/6
- 2017/5
- 2017/4
- 2017/3
- 2017/2
- 2017/1
- 2016/12
- 2016/11
- 2016/10
- 2016/9
- 2016/8
- 2016/7
- 2016/6
- 2016/5
- 2016/4
- 2016/3
- 2016/2
- 2016/1
- 2015/12
- 2015/11
- 2015/10
- 2015/9
- 2015/8
- 2015/7
- 2015/6
- 2015/5
- 2015/4
- 2015/3
- 2015/2
- 2015/1
- 2014/12
- 2014/11
- 2014/10
- 2014/9
- 2014/8
- 2014/7
- 2014/6
- 2014/5
- 2014/4
- 2014/3
- 2014/1
- 2013/12
- 2013/11
- 2013/10
- 2013/9
- 2013/8
- 2013/7
- 2013/6
- 2013/5
- 2013/4
- 2013/3
- 2013/2
- 2013/1
- 2012/12
- 2012/11
- 2012/10
- 2012/9
- 2012/8
- 2012/7
- 2012/6
- 2012/5
- 2012/4
- 2012/3
- 2012/2
- 2012/1
- 2011/12
- 2011/11
- 2011/10
- 2011/9
- 2011/8
- 2011/7
- 2011/6
- 2011/5
- 2011/4
- 2011/3
- 2011/2
- 2011/1
- 2010/12
- 2010/11
- 2010/10
- 2010/9
- 2010/8
- 2010/7
- 2010/6
- 2010/5
- 2010/4
- 2010/3
- 2010/2
- 2009/12
- 2009/11
- 2009/10
- 2009/9
- 2009/8
- 2009/7
- 2009/6
- 2009/5
- 2009/4
- 2009/3
- 2009/2
- 2009/1
- 2008/12
- 2008/11
- 2008/10
- 2008/9
- 2008/7
- 2008/6
- 2008/5
- 2008/4
- 2008/3
- 2008/2
- 2008/1
- 2007/12
- 2007/11
- 2007/10
- 2007/9
- 2007/8
- 2007/7
- 2007/6
- 2007/3
- 2007/2
- 2007/1
- 2006/12
- 2006/11
- 2006/10
- 2006/9
- 2006/7
- 2006/6
- 2006/5
- 2006/4
- 2006/1
- 2005/6
- 2005/5
- 2005/4
- 2005/2
- 2004/12
- 2004/11
- 2004/10
- 2004/8
- 2004/7
- 2004/6
- 2004/5
- 2004/2
- 2004/1
- 2003/12
- 2003/8
- 2003/7
- 2003/6
- 2003/5
- 2003/3
- 2003/1
- 2002/12
- 2002/10
- 2002/5
- 2002/4
- 2002/2
- 2002/1
- 2001/8
- 2001/5
- 2001/4
- 2001/2
- 2000/8
- 2000/7
RNAヘリカーゼによるグリシン作動性シナプス制御と行動制御
運動神経回路研究室(平田研究室)
J. Neurosci. 33: 14638-14644 (2013). doi: 10.1523/JNEUROSCI.1157-13.2013
RNAヘリカーゼと言えば、からまったRNA鎖をときほぐすための酵素と思われがちです。しかし実際のRNAヘリカーゼの機能はRNA合成、pre-RNAスプライシング、翻訳、リボソーム生合成、RNA分解など多岐に渡り、RNAが関わるあらゆる細胞内イベントに関わる酵素であると言えます。RNAヘリカーゼは6種類のサブグループ(DEAD box型やDEAH box型など)に大別され、ヒトでは計70以上のRNAヘリカーゼが同定されており、それらで全てのRNAイベントをカバーすると考えられています。いくつかのRNAヘリカーゼについては基質が報告されていますが、そもそも各RNAヘリカーゼに(E3ユビキチンリガーゼのような)基質特異性があるのか、各RNAヘリカーゼに固有の生理的機能があるのかなど不明な点が多く、RNAヘリカーゼの世界は謎に満ちています。
私たちはゼブラフィッシュの運動・行動異常を指標にして、グリシン作動性シナプス伝達に異常のある変異体をスクリーニングし、DEAH box型RNAヘリカーゼDhx37のゼブラフィッシュ変異体を得ました。電気生理学的解析から、Dhx37変異体ではグリシン作動性シナプス伝達が顕著に低下していることが分かりました。さらに詳細な解析から、Dhx37は特定のグリシン受容体αサブユニットのRNAに結合し、スプライシングを制御することで、グリシン受容体タンパク量、グリシン作動性シナプス伝達量を規定することが解明されました。この研究により、RNAヘリカーゼに明確な基質特異性・生理機能があることも確認されました。ヒトでグリシン作動性シナプス伝達の低下はhyperekplexia(通称:ビックリ病)という、突然の刺激による過剰な驚愕応答を特徴とする行動異常疾患を引き起こすことが知られています。家族性hyperekplexiaの原因遺伝子としてグリシン受容体遺伝子の変異が知られていますが、家族性で原因遺伝子が不明なものも依然多く、その解明が待たれます。今回の発見はDhx37がhyperekplexiaの新しい原因遺伝子であることを提唱するものでもあります。
また、細胞運命の維持にはH3K27のメチル化が関与する事が以前から知られていた。私たちは、ceh-22遺伝子へのHTZ-1の局在はH3K27脱メチル化酵素UTX-1の阻害で減少すること、HTZ-1とH3K27メチル化のゲノム上の局在には負の相関があることを示し、HTZ-1はUTX-1によってメチル化が除かれた場合に、転写抑制を行うことで細胞運命を維持している事を示唆した。H3K27のメチル化による安定した転写抑制と異なり、BET-1やHTZ-1は、分化を促すシグナルによって転写が簡単に誘導されるような遺伝子の、シグナルに依存しない転写を抑制していると考えられる。
この研究は関西学院大学・柴田博士、西脇博士との共同研究として行なわれました。
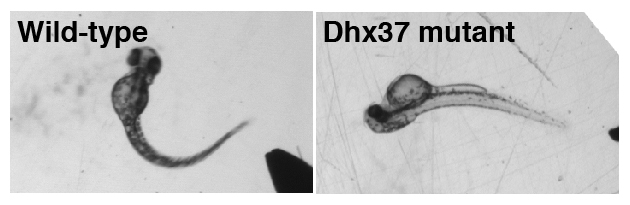
図:ゼブラフィッシュ稚魚をピンセットでつつくと逃避行動が見られ、正常な個体(Wild-type)の場合、体を側方に大きく曲げます。Dhx37に変異のある稚魚(Dhx37 mutant)の場合、体を側方ではなく背側に曲げます。これはグリシン作動性シナプス伝達に異常のある稚魚で特徴的に見られる左右同時の筋収縮によるもので、hyperekplexiaで見られる驚愕応答のサカナ版であるといえます。
野生マウスはどのようにして愛玩化されたのか
Tatsuhiko Goto, Akira Tanave, Kazuo Moriwaki, Toshihiko Shiroishi, Tsuyoshi Koide
Genes Brain and Behavior 2013. DOI: 10.1111/gbb.12088
人類はこれまでに様々な動物種を選択により家畜化してきました。その家畜化の過程で野生原種から変化する行動が愛玩化と呼ばれる行動形質です。しかし、この愛玩化とはどのような行動の変化であるのか、これまであまり明確にされてきていませんでした。私たちは、米国の動物学者であるEdward O. Priceが、その著書の中で、「愛玩化とは動物個体が人を避ける傾向が弱くなるか、あるいは積極的に人に近づく傾向が強くなること」と述べていることに着目しました。そこで、この二つの性質を区別するための3種類の行動テストを考案し、野生由来の10系統と実験用の6系統および愛玩用の1系統について、この新規行動テストを行いました。その結果、愛玩および実験用マウスは「愛玩化」の過程で、ヒトからの接触を避けないような行動特性が選抜されてきたものの、人に積極的に接近する性質については選択されてこなかったことが示されました。この結果は、今後の研究において、野生マウスがどのような遺伝的変化によって愛玩化されるか解明するための糸口になるものと期待されます。
なお、筆頭著者の後藤達彦博士は情報・システム研究機構、新領域融合プロジェクト特任研究員として研究に従事しました。
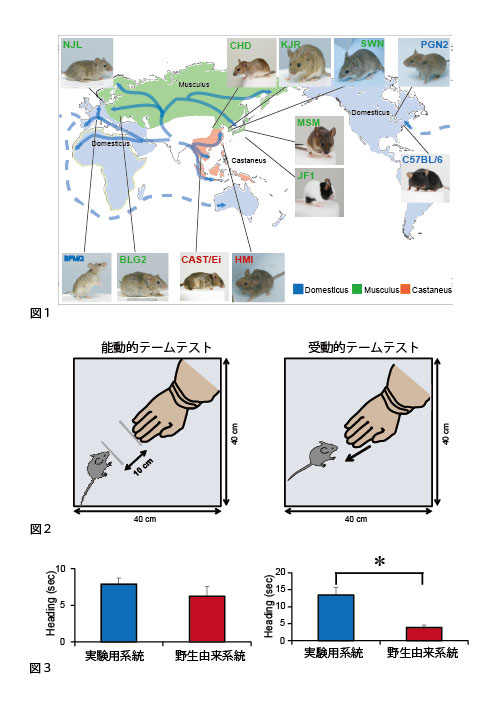
図1. 国立遺伝学研究所には、森脇和郎名誉教授を中心に世界各地で捕獲して収集し、それらから樹立された10種類の野生由来系統が維持されています。これらはいまだに野生マウスに特徴的な臆病な行動形質を保っており、世界的にも有数の貴重な遺伝資源です。一方、研究に一般的に使われる実験用系統は愛玩化されたマウスの集団から樹立されてきました。このように、野生系統と実験用系統はその由来も行動も顕著に異なるのです。
図2. マウスの愛玩化を調べるために新たに考案したテームテスト
図3. 実験用系統と野生系統は能動的テームテストでは有意な差を示さないのに対し、受動的テームテストでは野生由来系統がより人の手からの逃避を示します。
集団遺伝研究部門の斎藤教授が木村資生記念学術賞・日本進化学会学会賞を受賞
 表彰式日時:平成25年8月29日(木) 日本進化学会第15回つくば大会
表彰式日時:平成25年8月29日(木) 日本進化学会第15回つくば大会
 受賞題目:「近隣結合法などの分子系統進化学の方法論の開発とその応用研究」
受賞題目:「近隣結合法などの分子系統進化学の方法論の開発とその応用研究」
 日本進化学会サイト http://sesj.kenkyuukai.jp/special/index.asp?id=11632
日本進化学会サイト http://sesj.kenkyuukai.jp/special/index.asp?id=11632


集団遺伝研究系 集団遺伝研究部門 斎藤研究室
生態遺伝学研究室の石川麻乃研究員が日本進化学会第15回大会にて若手口頭発表最優秀賞を受賞

生態遺伝学研究室 北野研究室
酵母の日輪
Sho Okamoto, Kanji Furuya, Shingo Nozaki, Keita Aoki, and Hironori Niki
Eukaryotic Cell 2013 12:1235-1243. doi:10.1128/EC.00109-13
生物は太陽の光による昼夜の明暗サイクルから様々な影響を受けています。それは動植物のみならず、真菌や細菌においても同様です。私達は、真菌であるジャポニカス分裂酵母が、明暗のサイクルに応答すること発見しました。ジャポニカス分裂酵母は名前のとおり、日本で分離された酵母です。この分裂酵母は、栄養条件の悪化といったストレスやDNA損傷させるようなストレスを受けると、酵母から菌糸に生育の仕方が変化します。ペトリ皿の寒天培地の中心にこの分裂酵母を植えると、数日で酵母のコロニーが現れます(図a)。さらにこれを培養つづけると、コロニーの周囲から菌糸が放射状に伸長します(図b)。増殖中の菌糸に光を日周期的に照射させると、菌糸の部分に黒白の縞が形成されます (図c)。これは、ジャポニカス分裂酵母が、光の変化に反応したためです。この黒い縞の部分では、細胞分裂が一斉に活性していることがわかりました。真菌類では、WC-1とWC-2の2つのタンパク質からなる光受容体がよく知られています。確かに、これと類似したタンパク質の遺伝子がジャポニカス分裂酵母にもありました。それらの遺伝子を破壊すると光に応答しなくなるので、ジャポニカス分裂酵母でもWC光受容体が縞模様の形成時に働いていることがわかりました。さらに光だけなく、温度を上下すると光の刺激がなくても、同様の縞模様を作りだしました。この時には、WC光受容体は必要ありません。おそらく、別に温度の受容体があるのでしょう。以上のように、酵母も日周的に変わる温度や光といった環境要因を感知して、細胞の活動を周期的に調整することがわかりました。今後は、細胞分裂の活性化の仕組みや、熱受容体が何であるのかといった問題を解き明かしていきます。
なお筆頭著者の岡本尚 博士は、2012年度国立遺伝学研究所博士研究員制度の援助を受け、本研究を行いました。
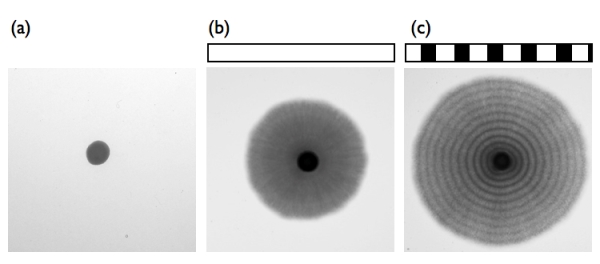
ジャポニカス分裂酵母は栄養ストレスのかかる培地で培養すると、数日間は酵母型の細胞で増殖し(a)のようなコロニーを発達させますが、さらに培養を続けると(b)のように菌糸型の細胞に転換し菌糸を伸長させるようになります。このときに明暗の刺激があると菌糸に(c)のような縞が形成されます(12時間の明条件、12時間の暗条件)。















