APCは紡錘体を引っ張る力のブレーキ がん抑制遺伝子APCの新しい機能の発見
![]()
Tumor suppressor APC is an attenuator of spindle-pulling forces during C. elegans asymmetric cell division
Kenji Sugioka, Lars-Eric Fielmich, Kota Mizumoto, Bruce Bowerman, Sander van den Heuvel, Akatsuki Kimura, Hitoshi Sawa
PNAS January 18, 2018 DOI:10.1073/pnas.1712052115
大腸ガン患者では高頻度でがん抑制遺伝子APCに変異があることが知られています。これは、Wntシグナルという細胞内シグナル伝達経路が過剰に活性化することが主な原因です。これに加えて、APCタンパク質は微小管を制御する働きが知られていますが、その働きと細胞のがん化との関係はよくわかっていませんでした。
本研究では、細胞の表層に局在したAPCタンパク質が、染色体の分配を担う紡錘体を構成する微小管の末端に結合して、微小管の安定性を制御していることが明らかになりました。APCタンパク質の微小管への結合は、微小管を引っ張る力を弱めることによって、染色体の移動を制御していたのです。
APC遺伝子が変異した大腸がん細胞では染色体異常が頻繁に観察されます。また、染色体異常は染色体の分配をおこなう紡錘体にかかる力の異常によっても引き起こされることが指摘されています。本研究で明らかになったAPCタンパク質の紡錘体を引っ張る力を制御する働きががん化に関与している可能性があります。
本研究は、情報・システム機構国立遺伝学研究所の元研究員杉岡賢史、澤斉教授と同研究所細胞建築研究室およびユトレヒト大学、オレゴン大学との国際共同研究の成果です。
本研究成果は、米国科学誌「米国科学アカデミー紀要(PNAS)」に平成30年1月18日(米国東部標準時間)に掲載されました。
本研究は、科学研究費補助金(JP22127005、JP15H04732 、JP15KT0083)上原記念生命科学財団および遺伝学研究所共同研究(NIG-JOINT:2013-A60)の支援を受けておこなわれました。
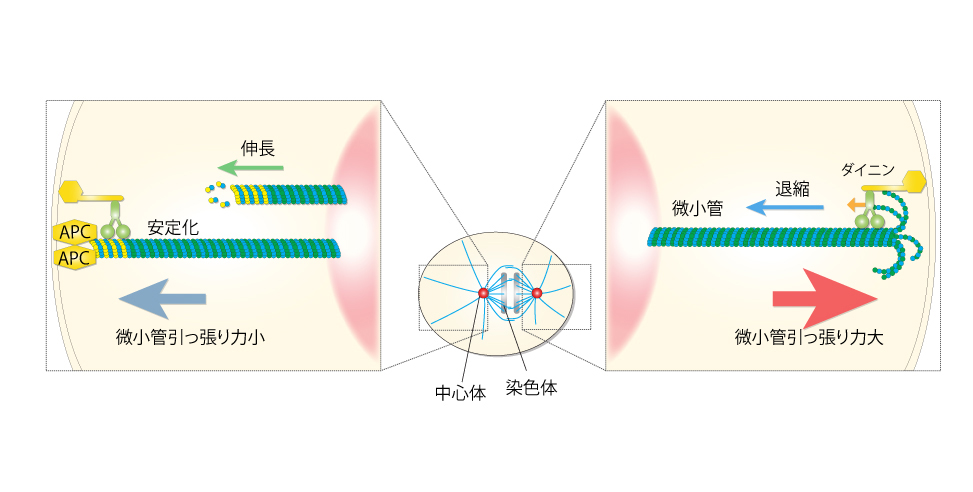
図:APCタンパク質による微小管引張り力の抑制機構
微小管が細胞表層に到達した後、退縮する際に、モータータンパク質であるダイニンの働きで引っ張る力が発生する。APCタンパク質が微小管の末端に結合することで退縮を阻害し、引っ張る力を弱める。
線虫の非対称分裂の動画をこちらでご覧いただけます
右:野生型では後極から強く引っ張られるため紡錘体が後方に移動する。この際、後ろ側の中心体は、強い力を受けて縦方向に振動する。前極に局在するAPCが引っ張る力を抑制するため前側の中心体はほとんど動かない。左:APCを阻害すると、前方の中心体も振動する。















