マウス生殖細胞の雌化因子を同定(卵巣内で精子分化開始)
![]()
Sexual Fate Change of XX Germ Cells Caused by the Deletion of SMAD4 and STRA8 Independent of Somatic Sex Reprogramming
Quan Wu, Kurumi Fukuda, Yuzuru Kato, Zhi Zhou, Chu-Xia Deng, Yumiko Saga
PLOS Biology September 8, 2016 DOI:10.1371/journal.pbio.1002553
ヒトを含め哺乳動物の性は性染色体の構成によって決まります。XX染色体を2本もつ個体は雌になり、卵巣の中には卵子ができます。一方、XY染色体をもつ個体は雄になり、精巣の中で精子が形成されます。精子や卵子の元となる始原生殖細胞は卵巣や精巣とは別の場所でつくられ、胎児期の間に移動して、精巣あるいは卵巣に入るかで、将来精子を作るか卵子を作るかの運命が決まります。すなわち、生殖細胞の性は周りの環境によって決まるのです.しかし、そのメカニズムはよくわかっていませんでした。我々は以前、生殖細胞の雄化にはNANOS2というRNA結合タンパク質が必須であることを示していますが、雌化の仕組みは不明でした。
今回の研究では2つの因子SMAD4とSTR8を卵巣の生殖細胞のみでノックアウトすると周りの環境はメスであるにも関わらず、生殖細胞は雄化してNANOS2などの雄性遺伝子を発現し、精子前駆細胞とよく似た性質を示すことがわかったのです。従って、これらの2つの因子は生殖細胞を雌化する因子であり、これらの因子がないと生殖細胞は雄化することがわかりました。
最近、培養系でES細胞や、iPS細胞から始原生殖細胞を誘導できることが報告されていますが、その後の性分化には体細胞環境が必須です。今回の研究成果は、体細胞なしに、生殖細胞の性分化を操作できる可能性を示唆しています。またこれまで、精子の形成にはY染色体の下流因子が必須であると考えられてきましたが、今回の結果は生殖細胞の雄化には、そのような雄特異的な体細胞因子は必要ではないことを示唆しています。この研究は、「新学術領域研究:生殖細胞のエピゲノムダイナミクスとその制御及」び「基盤研究A」の支援を受けています。また筆頭著者の呉泉は総研大遺伝学専攻出身者で現在は神戸CDBで研究を続けています。
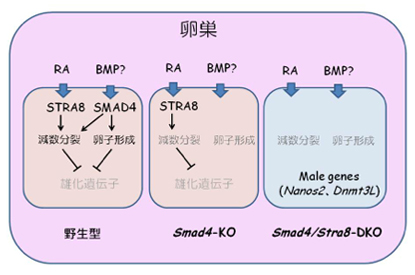
野生型の胎児卵巣の体細胞から分泌されるRAとBMPシグナル(仮説)がそれぞれ生殖細胞のなかでSTRA8とSMAD4を介して、雌化を誘導する。SMAD4単独のノックアウトでは性転換は起こらない。しかしこの2つの遺伝子がKOされると、減数分裂、卵子形成は完全にブロックされて、雄化がおこる。
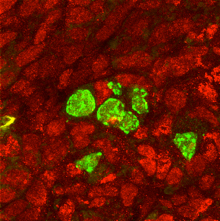
Smad4/Stra8ダブルノックアウト生殖細胞が卵巣の中で雄性因子PLZF(緑)を発現。赤は、卵巣体細胞特異的FOXL2の発現。















