Nanos2によるmRNAの転写後調節が精子幹細胞の維持に重要
The RNA binding protein Nanos2 organizes a post-transcriptional buffering system to retain primitive states of mouse spermatogonial stem cells
Zhi Zhou, Takayuki Shirakawa, Kazuyuki Ohbo, Aiko Sada, Wu Quan, Kazuteru Hasegawa, Rie Saba, Yumiko Saga Developmental Cell. Published Online: June 25, 2015 DOI:http://dx.doi.org/10.1016/j.devcel.2015.05.014成人男性が50年以上の長期間にわたって精子形成を継続的に維持できる理由は、精子幹細胞が自己複製と精子形成をバランスよく調整しているからである。我々はマウスの精子形成過程をモデルとしてその維持機構の解析を続けている。以前にRNA結合タンパク質Nanos2が精子幹細胞の維持に必須であることを明らかにしてきたが、その詳細な分子機構は不明であった。今回、Nanos2は主に2つのメカニズムで精子幹細胞の未分化性を維持することを明らかにした。ひとつは、Nanos2がP-bodyとよばれるmRNA-タンパク質複合体に標的となる分化促進mRNAをリクルートして、その分解及び翻訳抑制を介して発現を抑制することでその主な標的としてSohlh2 mRNAを同定した。またNanos2は, 細胞増殖や分化を促進するmTORCシグナル系のコア因子mTORと結合し、その機能を抑制することで未分化性を維持することを明らかにした。これらの機能はNanos2の発現量に依存しており、Nanos2がmRNPの機能を制御する緩衝因子として機能していると結論づけた。 本研究は、科研費「新学術領域研究:生殖細胞のエピゲノムダイナミクスとその制御」及び、融合研究「データ同化」の支援を受けています。また筆頭著者のZhi ZhouはH24年度遺伝研ポスドクとして採用されています。
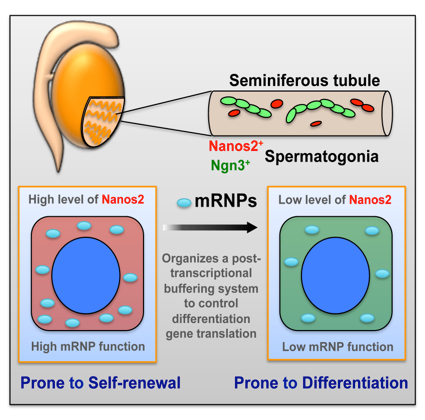
Nanos2はmRNPの形成を介して精子幹細胞の未分化性を維持する。Nanos2の発現が高い細胞は、多くのmRNPが形成され、分化関連遺伝子やmTORCシグナルの抑制を介して分化抑制する。















