第18回 長生き遺伝子の謎を解く

長生き遺伝子の秘密を突き止めたのですね?
そうなのです。サーチュイン遺伝子は、寿命を伸ばす効果があって、長生き遺伝子としてとても有名。でも、どうして寿命が伸びるのか、その仕組みは謎でした。いろいろな人がいろいろな可能性を提唱してきたけれど、正解はわからなかった。たとえば、染色体のテロメアに関係するとか、タンパク質繊維のアクチンに関係するとか、さまざまな説があったのです。
ところが今回の私たちの研究で、そうした可能性は、正しいかどうか以前に、そもそも重要でないとわかりました。私の仮説が正しく、しかも決定的だと判明したからです。
小林先生はどうお考えでしたか?
サーチュイン遺伝子はリボソームRNA遺伝子の数(コピー数)を制御している、というものです。サーチュイン遺伝子にこうした働きがあることは、すでに私たちが発見していました。でも、それが、サーチュイン遺伝子の長生き効果における唯一の重要な作用で あるということは、今回の研究で初めて確認できたのです。
世の中には、サーチュイン遺伝子を活性化する健康補助食品などが出回っていますが、今後、リボソームRNA遺伝子のコピー数を安定させる健康補助食品なども、開発されるかもしれませんね。
そもそもリボソームRNA遺伝子とは、どういう遺伝子ですか?
細胞中にはリボソームと呼ばれる細胞小器官が含まれており、タンパク質の製造工場として働いています。 このリボソームの構成材料の1つがリボソームRNAで、リボソームRNAを作る遺伝子が、リボソームRNA遺伝子です。遺伝子というとタンパク質を作るこ とがイメージされますが、RNAを作る遺伝子もあるのです。
リボソームRNA遺伝子は特殊な遺伝子で、同じ遺伝子が何個も並んで存在します。つまりコピー数が多い。ゲノム中に100個以上もあります。同じコピーがたくさん並んでいる遺伝子には、DNA複製や修復などのときに、いわば場所の取り違えが起こりやすく なります。そしてその取り違えの結果、遺伝子のコピー数の変動が起こるのです。
サーチュイン遺伝子は、こうしたリボソームRNA遺伝子のコピー数が変動しないように調節する働きをしています。
どのようにしてコピー数を調節するのですか。
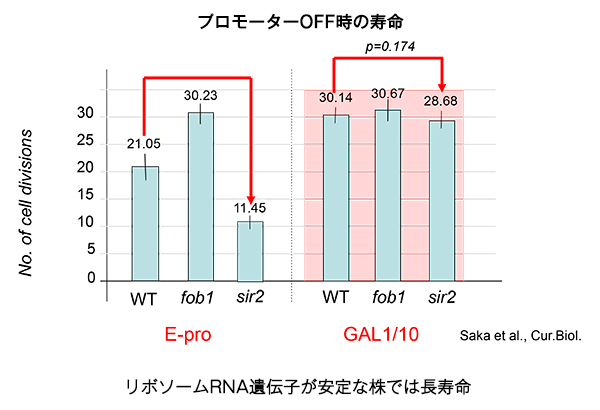
具体的には、サーチュイン遺伝子から作られたサーチュインタンパク質Sir2が作用します。そもそもゲ ノム中には、リボソームRNA遺伝子に隣接して、E-proという名前のプロモーター配列が存在しているのですが、このE-proが活性化すると、リボ ソームRNA遺伝子のコピー数が増加されます。サーチュインタンパク質Sir2は、このE-proを制御することで、リボソームRNA遺伝子のコピー数を 制御しているのです。
今回の実験では、酵母のE-proを欠損した変異株を用いました。そして、誘導可能なE-pro代替物(GAL1/10)を導入し、その活性を自由に調節できるようにしたのです。研究では、いろいろな条件下における酵母の寿命を測定することで、サーチュイ ン遺伝子(タンパク質)の働く仕組みを解明できました。この人工的なE-pro代替物は便利で、これを調節することで、酵母の寿命の長さを自由に操作する ことまで可能になったのです。
酵母は老化の研究によく用いられていますね。
酵母は、単細胞の真核生物です。一世代が長い高等動物に比べ、実験が比較的簡単で短期間。何年間も観察 する必要がありません。また、飼育係の愛情が動物の寿命に影響すると指摘されていますが、そうした心配も不要です(笑)。実は、酵母とヒトには共通する因 子や遺伝子が多いので、酵母がヒトのモデル生物になるということもありますよ。サーチュイン遺伝子が最初に発見されたのも、酵母においてでした。ですか ら、今回の酵母での研究成果は、ヒトでの研究にも大きな刺激を与えるものだと思います。
とはいえ、それでも実験は大変なのですけれどね。数マイクロメートルの酵母を顕微鏡下で観察し続け、どの酵母細胞が分裂したかを追跡しなくてはいけないからです。眼が非常に疲れるし、根気と忍耐がいる。今回の研究では、坂 季美子技術職員がその観察にあたってくれましたが、研究の成功は彼女のおかげです。
老化と寿命の関係は、どうとらえたらいいでしょうか?
酵母の場合ですが、2時間に1回くらいの割合で細胞分裂を行い、娘細胞を作っています。その分裂が15 回くらい繰り返されると細胞分裂の速度が遅くなり、約20回を過ぎると分裂が止まって、2日間の命が閉じられます。細胞分裂の回数が、酵母の寿命(正確に は分裂寿命と呼ばれます)になっています。
人工的に酵母の寿命を延ばしてみると、細胞分裂の回数は30回くらいまで増やすことができます。しか し、このときにゲノムを調べると、ゲノムのさまざまなところに突然変異が生じているのがわかります。これからいえることは、寿命が伸びると、異常な細胞が 増える。多細胞生物ではいえば、がんを発生させていることになるわけです。ゲノムの状態をチェックし、異常が出る前に細胞の増殖を停止させる機構、すなわ ち寿命をもたらす機構が老化というわけなのです。つまり老化は重要な生理現象ということができます。そして、ゲノム中のリボソームRNA遺伝子が存在する 場所は、コピー数が変動しやすい、不安定な場所です。ですから、この部位はゲノムの状態を調べるセンサーのような働きをしているのではないか、という仮説 を私は立てたわけです。
老化には、ゲノムの状態だけでなく、ほかにも、細胞や個体の別な側面のチェック機構があるでしょう。私はそのなかの、ゲノムという側面について研究していることになります。
今後の研究はどういう展開に?

リボソームRNA遺伝子のコピー数の増減を検知する仕組みについては、まだわかっていません。リボソー ムRNA遺伝子から発せられるシグナルがあるはずです。それがわからないと、本当の意味で全体像が明らかになったことにはならないと思いますから、まずこ れを研究するつもりです。
また、酵母は、ヒトの幹細胞研究のモデルにもなっています。酵母細胞が分裂すると娘細胞と母細胞ができるのですが、娘細胞は若返るので、それが幹細胞のモデルになるのです。老化の研究を、幹細胞の研究に活かしていきたいとも考えています。
(文: サイエンスライター・藤川良子 / 2013.9.02掲載)
Cellular senescence in yeast is regulated by rDNA noncoding transcription.
Kimiko Saka, Satoru Ide, Austen R.D. Ganley, and Takehiko Kobayashi
Current Biology, 29 August 2013 doi:10.1016/j.cub.2013.07.048















