


網膜に入った視覚刺激は、神経の信号に変換されて脳に送られる。このとき、網膜は視覚対象物の色や形、動きなどを要素別の信号にしているが、米原教授は、対象物の動きの方向を検知する仕組みを解明し、この研究分野の突破口を開いた。
Profile
2003年 東京大学農学部獣医学課程卒業。2008年 総合研究大学院大学/基礎生物学研究所 博士(理学)取得後、同研究所にて博士研究員。2009年 フリードリッヒ・ミーシャー生物医学研究所(スイス) 博士研究員。2015年 オーフス大学医学部ダンドライト研究所(デンマーク)准教授/北欧EMBLグループリーダー、2021年10月より、国立遺伝学研究所(遺伝研) 教授。
思ったようにいかないスタート

私の研究の原点は、大学院時代にさかのぼります。それは、マウスの網膜の神経回路での発見でした。
東京大学の獣医学課程を修了した私は、2003年、基礎生物学研究所の野田昌晴教授の研究室に大学院生として加わりました。本好きの私は、利根川進先生が『精神と物質』(文春文庫、1993年刊)という本の中で、大学院進学先を探すのに日本中を訪ね歩いたと書いているのを読み、自分も実際に何カ所かの研究室を訪ね、進学先選びにエネルギーを注いだものです。そうして選んだ野田研究室は、分子生物学の実験技術を軸に、神経の回路を解明したいと思っていた私にぴったりの研究室でした。
意気揚々とスタートをきったはずの博士課程でしたが、あいにく当初は苦しい時間の連続でした。網膜から脳へ伸びる神経回路で働く遺伝子群を調べていたのですが、思うようなデータが得られなかったのです。頭を抱える日々が続きました。研究者を諦めようかという思いさえ、何度も心の中をよぎりました。
しかし、あるとき幸運の女神が訪れてくれました。他の目的でしかし、あるとき幸運の女神が訪れてくれました。他の目的で解析していたマウスの遺伝子が、重要な発見につながることとなったのです。
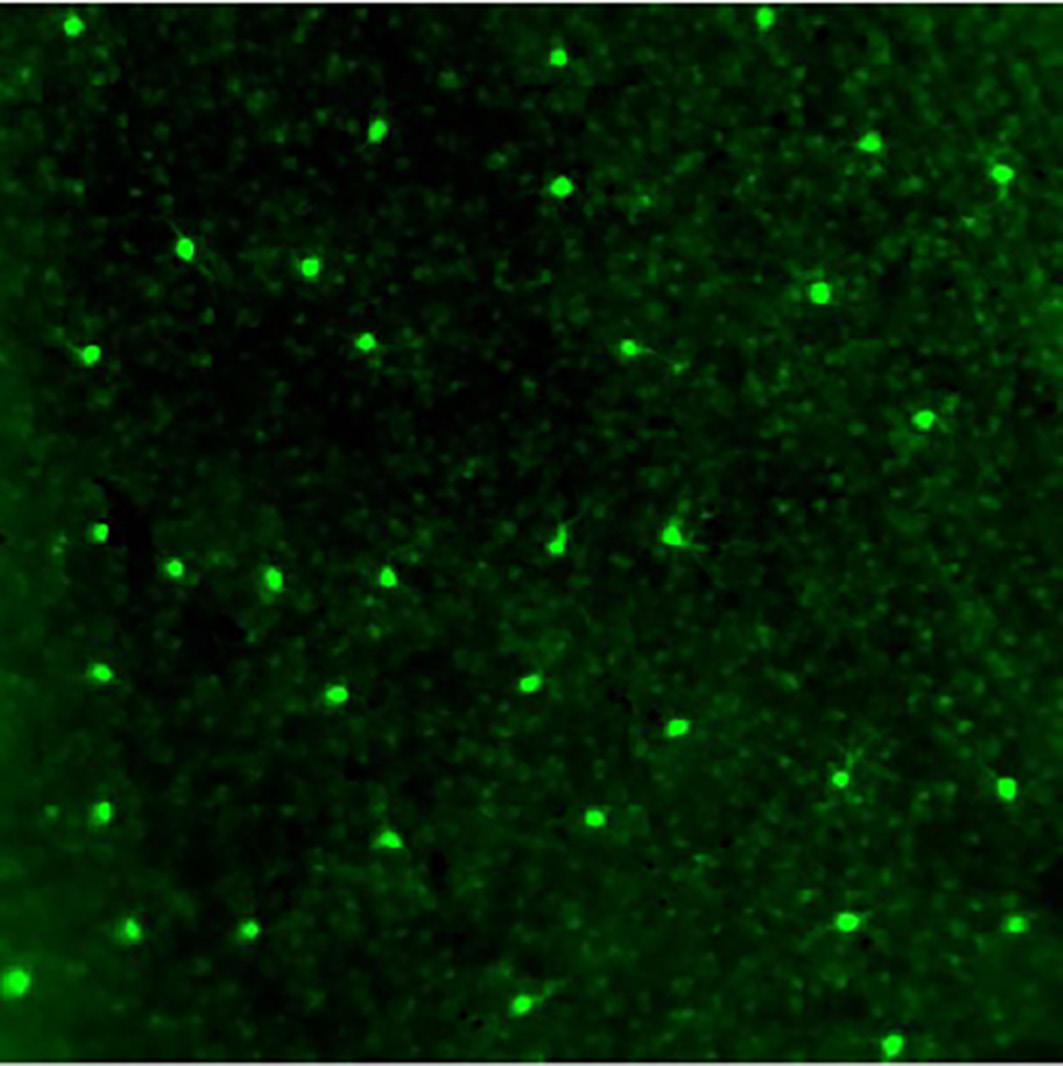
それは、SPIG1という遺伝子が、網膜でどのような発現パターンを示すかを調べていたときのことです。その遺伝子には、発現すると緑色蛍光タンパク質(GFP)が蛍光を発するような処理が施してあります。網膜の顕微鏡画像を見ていた私は、そのGFP標識の蛍光がモザイク状に現れていることに気がつきました。網膜上にポツポツと、互いに離れた場所の細胞に等間隔に現れているのです。このGFP標識は、網膜に含まれる細胞の何か重要な特徴を捉えている可能があると考えた私は、急遽、博士論文の研究テーマをこの細胞の解析に変更することを決断しました。
方向選択性細胞を標識する
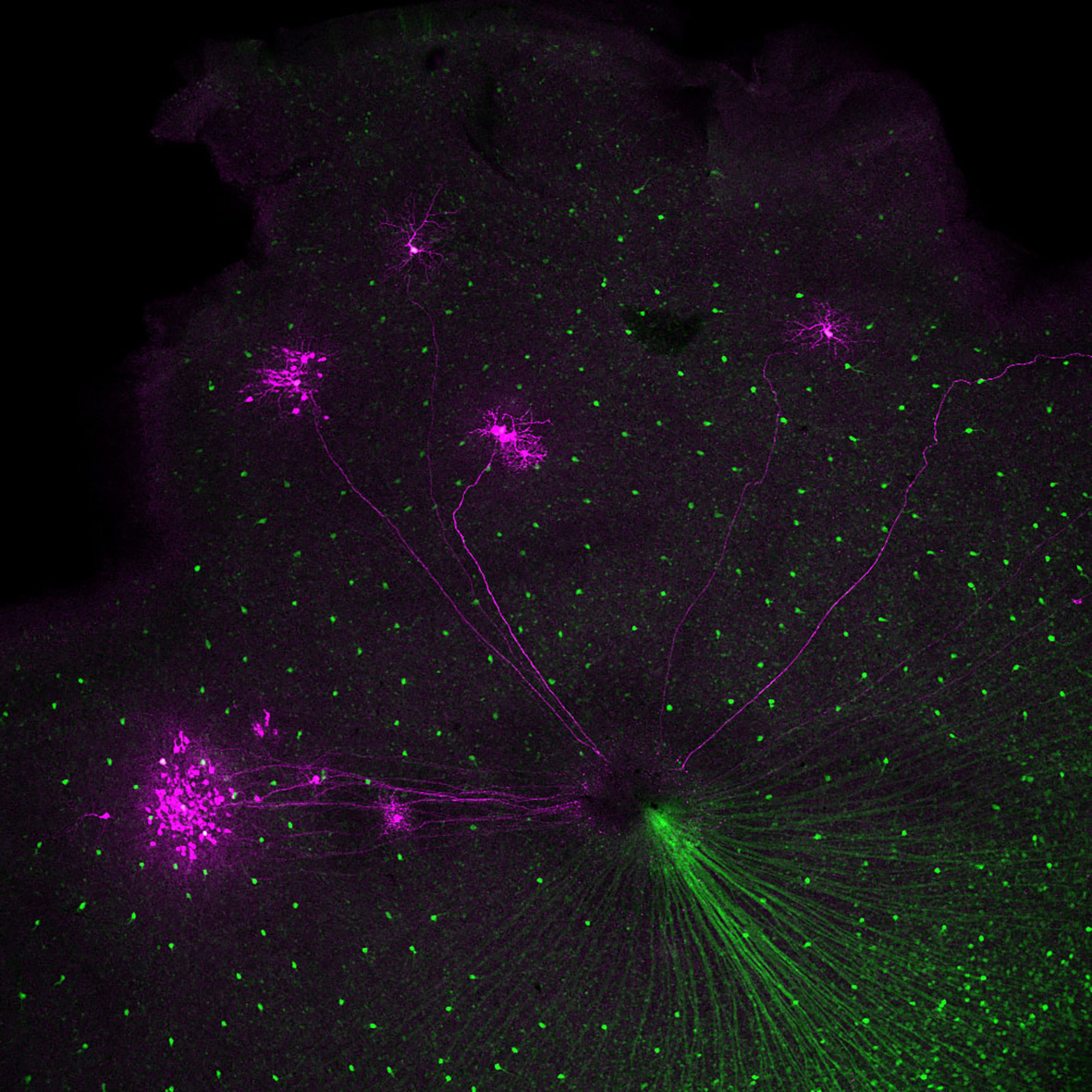

眼の網膜は、光を受容する器官です。そこで受け取った視覚刺激は、網膜から脳へと送られます。私は、網膜で蛍光を発していたGFP標識細胞が、脳のどこに伸びていくのかを見てみました。すると、「副視覚系の内側核」という脳の部位に伸びているように見えました。
この「副視覚系の内側核」に関する過去の文献を調べてみると、そこは視覚の「方向選択性(上・下方向)」に関与する、と記されています。では、「方向選択性」とは何でしょうか。それについて述べる前に、網膜の視覚回路の特徴について説明しましょう。網膜が受け取った視覚刺激は、見る対象物の色や形、距離、動きの方向や速度といった要素ごとの信号に抽出されて、脳へと送られることが知られています。視覚は、景色一体を漠然と捉えるのではなく、生物にとって重要な情報を選択的に検知して捉えているわけです。
では、視界の中の対象物が動いているということは、どのような仕組みで検知されるのでしょうか。古くからの研究で、一定の方向の動きにだけ選択的に反応して信号を脳へ送る細胞が網膜に存在することが知られていました。仮に、動きの方向として、上下左右の4つの方向を考えたとしましょう。対象物が上方向に動いたときにだけ選択的に反応する細胞や、下方向、あるいは右方向、左方向に動いたときにだけ選択的に反応する細胞が存在するということです。こういう性質が「方向選択性」と呼ばれているのです。
私は、網膜のGFP標識細胞が方向選択性をもった細胞かもしれないと考え、それを確かめるために、今度は逆に、脳から網膜へと神経回路をたどってみました。それには逆行性トレーサーという染色技術を使います。その結果、確かに内側核から網膜の神経節細胞にたどりつくことが確認できました。
ここで非常に驚いたことがあります。脳からたどって網膜に到着したもののうち、半分はGFP標識細胞と一致しました。ですが、残りの半分はGFP標識細胞ではありませんでした。ということは、脳の内側核へは、GFP標識細胞だけでなくGFP非標識細胞からも回路が伸びていたことになります。それならば、GFP標識細胞とGFP非標識細胞は、一方が上方向で、もう一方が下方向の選択性をもつのかもしれない。つまり、このGFP標識によって、どちらか1種類の方向選択性をもつ細胞を特定できるはずだ。そう気づいた私は、これは重要な発見になると身震いしました。暗室で共焦点顕微鏡をのぞき、びっくりして飛び上がったその瞬間を、今でも鮮明に覚えています。
博士学位審査を間近に控え、急ぎ論文化
の発見が正しいことを証明するためには、電気生理学的手法による実験を行うことがさらに必要でした。しかし、これは野田研究室では用いていない手法でしたので、理化学研究所の石金浩史先生(現在 専修大学教授)に共同研究を申し込み、GFP標識細胞が、実際に視覚刺激の運動方向に応答することをマウスで調べていただくことにしました。
一方で、大学院博士課程の修了時期が迫っていました。そのタイミングから逆算すると、この研究を学位論文に仕上げる時間的余裕はあまりありません。そこで泣く泣く論文は2回に分けて発表することにしました。まず、電気生理学的実験の結果を待たずに、方向選択性細胞を発見したこれまでの結果を論文にまとめたのです。これが、2008年にPLoS Oneに掲載されました(*1)。
その後、電気生理学の実験結果は、期待通りのものが得られました。GFP標識細胞が方向選択性をもつ細胞であることを実証するとともに、それが上方向の運動にのみ反応することを確認できたのです。こちらの論文は、翌2009年のPLoS Oneに掲載されました(*2)。
この2つの論文に対する反響が非常に大きいものであることは、米国神経科学会でのポスター発表での手応えから伝わってきました。国際的論文評価システム(F1000)では、「Must Read」の論文にも選ばれました。
この研究成果の意義は、2つあると思っています。1つは、SPIG1遺伝子を利用して細胞をGFP標識すれば、方向選択性の解析を行えるようになったことです。この遺伝子は、マウスの胎生期から発現するので、網膜の方向選択性がどのように発達するかを調べる手段ができたのです。F1000では、「網膜の神経細胞を遺伝学的に解析する新たな分野を切り開いた」という評価をいただきました。
もう1つの意義は、この上方向の方向選択性が遺伝的に運命決定された細胞だとわかったことです。神経系の細胞は、経験を通じて特定の性質を獲得していく例がたくさんあります。方向選択性をもつ細胞も、そのタイプである可能性も考えられていましたが、そうではないことをこの研究が実証しました。
本に助けられる


野田研究室での大学院時代には、研究の内容とは別に、研究の心構えというものの大事さも教わりました。それこそ大学院時代に身に着けるべき最も大切なものだったのかもしれないとも思います。私は当初、自分の考えにとらわれがちで、人の意見をあまり聞かないこともありました。しかし、コミュニケーションや自ら心を開くことが研究において、おそらくどんな仕事においても、非常に大切であることを野田研究室で学びました。
先ほども本好きだと言いましたが、若いときはそれこそ、研究と寝るとき以外は本を読んでいた人間です。悩んだときや躓いたときには、本に答えを求めることも多くありました。現実の社会では、自分の周囲には限られた人しかいませんが、本を介せば、いろいろな著者にアクセスできます。過去の賢い先人たちが言いたいことを濃縮した文章から学ばないのは、損だと思うのです。
例えば、大学院時代に最も強く影響を受けた言葉には、ドラッカー(PeterDrucker)の著書からの「有能さは習得できる」があります。それまでは人の有能さは生まれつきや教育によって決まってしまい、あとは知識を増やすくらいしかないと思っていたのですが、この言葉に出会って、自分を変えようと思いました。物事を自分がどう考えて、どう応答するかといったことをより客観的に眺め、どう行動すべきかを判断するように心がけました。
その後のポスドク時代に読んで、特に印象に残っているのは『ゲーテとの対話』(岩波文庫、1968-69年刊)です。一流になるにはどうしたらよいか、ということが書いてあったのです──新しいものを作り出したいならば、先人に学ばなければいけない。過去の積み上げのなかにしか、新しいものはない。独創性を求めて、独りよがりになってはいけない──こういった言葉が、私の行動の指針になりました。
ロスカ研究室で引き続き研究を発展させる
博士課程を修了した後も、私は網膜における方向選択性の解析をさらに発展させていきたいと考えました。博士研究員として参加するにはどこがいいか、いろいろ調べた結果、スイスのロスカ(Botond Roska)研究室が最適だと考えました。ロスカ研究室は、当時バーゼルのフリードリッヒ・ミーシャー生物医学研究所にありました(その後、バーゼルに分子臨床眼科学研究所を創設し、そこの所長となっています)。ロスカ博士は、二光子顕微鏡を使って哺乳類の網膜の光応答を初めて記録したうちの1人です。研究室には、網膜の神経回路の研究に重要な二光子顕微鏡、電気生理学的技術のほか、ウイルスベクター、そして、当時まだ珍しかった光遺伝学の技術まで揃っていました。
すぐさま私は、GFP標識細胞を使った研究のアイデアをしたためたアプリケーションレターをロスカ博士に送りました。すると、すぐに面接に呼ばれ、採用が決定しました。そして野田教授は、GFP標識マウスを持っていくことを快く許してくださいました。
ロスカ研究室に着任したその日に、私はロスカ博士と6時間ほどディスカッションし、研究テーマをいくつか決めました。細胞が方向選択性という信号を獲得するには、どのような仕組みが考えられるでしょうか。これまでの研究により、網膜を構成する神経節細胞が周囲の細胞から受け取る信号(入力信号)は、空間的に非対称的であることがわかっていました。そして、この非対称性が方向選択性をもたらす仕組みだろうと推測されていたのです。ロスカ博士に送ったレターで私は、非対称的な入力信号がマウスでどのように発達していくのかをGFP細胞を用いて調べれば、方向選択性獲得の仕組みを実証できるというアイデアを説明したのでした。それが、最初に取りかかる研究テーマになりました。そのための具体的な実験方法は、ロスカ博士がアイデアをくれました。光遺伝学と電気生理学、二光子顕微鏡を使った方法です。
私はこれらの技術を自分で実験に使えるように習得し、実験に取りかかりました。網膜には、受容した視覚刺激を神経節細胞に送る「スターバーストアマクリン細胞」と呼ばれる細胞があります。この細胞からGFP標識細胞への入力を調べると、生後6日目までは、どの方向からの視覚刺激に対しても信号が入力しますが、生後2週間目に入ると、一定方向(上方向)の視覚刺激に対してのみ信号が入力することがわかりました。つまり、信号の空間的非対称性の発達する様子を明らかにし、網膜の神経節細胞に方向選択性を付与していることを証明したのです。
研究結果は、2011年にNatureに掲載されました(*3)。2008年と2009年のPLoS One掲載論文で始まった一連の研究が、これで一段落したという思いでした。
ロスカ研究室時代の研究には、私の代表的論文と捉えてくださる人の多い、2016年にNeuronに発表したものもあります(*4)。空間的非対称性に必須の遺伝子がFRMD7であることを突き止めた以下の研究です。
GFP標識に利用しているSPIG1遺伝子ですが、これは単にこの細胞の標識に利用できるだけで、方向選択性(や信号の空間非対称性)をもたらす原因とは無関係であることが、早い段階からわかっていました。ではどんな遺伝子がこの仕組みに必須なのか、それを探す研究が競争になっていました。
私がFRMD7遺伝子を見つけたきっかけは、ある遺伝病です。私たちの眼は、例えば電車に乗って移動時に窓の外を眺めると、流れる景色に追従するような動きをします。これは視野を安定化させるために起こる眼球の自然な反射運動なのですが、先天性眼振という遺伝病の人では、この反射運動が起こらないことが知られています。そして、この遺伝病の7割の人は、FRMD7遺伝子の欠損が原因で、この病気が引き起こされるのです。
あるとき、ロスカ研究室の実験結果をまとめたデータベースを眺めていたときのことです。網膜のスターバーストアマクリン細胞が、このFRMD7遺伝子を発現していることに気づきました。もしかしたら先天性眼振という病気は、網膜の方向選択性細胞が障害されている病気なのかもしれない。そのことをロスカ博士に伝えると、教授も興奮し、二人でそのままマウス飼育施設に行き、FRMD7遺伝子を欠損させたノックアウトマウスを作る手はずを整えました。そしてこのマウスを解析した結果、このマウスは、水平方向の運動を認識する方向選択性が失われていることがわかり、FRMD7がその原因であることを明らかにできたのです。
この遺伝子の発見には、もう1つ大きな意義がありました。それ以前は、網膜の細胞が方向選択性をもつのは下等な哺乳類およびその他の脊椎動物だけと思われていたのです。しかしそうではなくて、ヒトの網膜にも存在するだろうという推察の、初めての強い根拠になったのが私の研究でした。これ以降、霊長類の網膜での方向選択性の解析が盛んに行われるようになりました。
独立して自分のラボをもつ


ロスカ研究室では良い論文がたくさん書けましたし、ロスカ博士の研究に対するビジョンからも多くを学ばせていただきました。次は、いよいよ自分自身のラボをもつ段階だと考え、準備を始めて、ポジションの応募書類を、世界中50カ所くらいに送りました。
いくつかの研究所から良い返事が来たのですが、私は迷わずデンマークのオーフス大学に行くことに決めました。スタートアップ(研究室立ち上げ)に用意されている金額が飛び抜けて多かったからです。網膜に関する私の研究では、二光子顕微鏡が必要になります。独立するにあたり、この高額な顕微鏡を新たに購入しなくてはいけないので、スタートアップの額の多寡が最優先課題だったのです。私は、自分がどう行動していくかを計画するのが好きですし、自分にとって何が最適かをその都度考え、行動を選択します。自分にとって一番大事だと思うこと以外のことに迷わされることは少ないです。
2015年、私はオーフス大学医学部のダンドライト研究所に、准教授および北欧EMBLグループリーダーとして着任しました。二光子顕微鏡は、エネルギーの低い近赤外光で蛍光色素を光らせる仕組みを用いているので、視野がまぶしくなり過ぎることがなく、標識細胞が光にどう応答していくかを記録する実験が行えるようになります。この顕微鏡を自分たちの研究室で所持できる。こんなにうれしいことはありません。自分たちの顕微鏡であれば、システムを修正して、例えば光刺激の波長を微調整したりして、自分たちに適した装置に改良できるのです。
オーフス大学での研究成果は、まだ論文にできていないものもあるのですが、発表済みのいくつかを紹介しましょう。副視覚系に信号を送るタイプの方向選択性細胞は、見る対象物の速度が遅いときには強く反応し、速度が速いときにはあまり強く反応しないという傾向があり、この速度依存性が視野安定化のための眼球の反射運動の制御に重要なのですが、その仕組みを解明しました(*5)。
また、網膜を構成する細胞の中には、「双極細胞」という種類もあります。これが方向選択的な信号を発するかどうか、よくわかっていませんでした。ロスカ研究室時代にもこの研究を行い、そのときには「発しない」という結論だったのですが、ここでの解析からは、それを覆す実験結果が得られました(*6)。シナプス1個1個の反応を二光子顕微鏡で測定し、その大量のデータを機械学習で解析したのです。より精度の高い解析を行ったことで得られた結果だと考えます。これ以外にも、網膜からのシグナルが大脳皮質のどの領域に届くのかを、FRMD7ノックアウトマウスを使った解析によって見つけたこともありました(*7)。
ヨーロッパでグラントを獲得する

オーフス大学で自分の研究室を立ち上げたときには、大学から得られるスタートアップの資金のほかにも、グラント(研究助成金)を獲得しました。ポスドク時代のものも含め、ヨーロッパの研究助成金について説明します。
ヨーロッパでポスドクとして研究するときに大事なフェローシップが4つあります。ヒューマン・フロンティア(Human Frontier Science Program Long-term Fellowship)、マリー・キュリー(Marie Skłodowska-Curie Individual fellowship)、EMBO(EMBO Long-Term Fellowship)、そして海外学振(日本学術振興会の海外特別研究員)制度です。私はそのうち、EMBOフェローシップと海外学振制度に採用されました。
また、独立した研究者のためには、ヨーロッパにおける大規模な研究助成機関である欧州研究会議(ERC)のものがあります。ERCは、研究者のキャリアのステージごとに助成金を用意しており、競争率が非常に高いグラントです。幸運にも私はこのStarting Grantsに採用されました。オーフス大学で研究室を立ち上げたときには、この助成金とオーフス大学のスタートアップとを合わせた資金を利用することができたので、たいへん助かりました。
このERCの研究助成金には、独立先の大学のポジションが決まってから応募できます。面接を含め審査には1年程度かかりました。応募書類を書くにあたっては、まず、過去の助成金獲得成功者の申請書を3~4人分集め、どのように書くのかを学びました。その上で書きあげた申請書を、今度はノーベル賞受賞者を含めた何人もの人に読んで批判してもらい、改良していきました。審査が順調に進むと、次に面接があります。15分ほど発表した後、5分程度の質疑応答です。面接の練習ももちろん怠りませんでした。
私が面接の練習に最もエネルギーを注いだのは、ロスカ研究室後の独立研究者の職を得ようとしたときでした。ヨーロッパの大学ですと、候補者が6人程度集められ、シンポジウム形式で30分くらい発表する、という形式の面接が多いと思います。毎日、何度も何度も練習し、その後、皆の前で発表し、批判をあおいで修正するということを繰り返しました。発表をビデオで撮影し、それを見直して、発音や身振り手振りを確認することも行いました。オーフス大学のほかに複数の大学の面接を受けたのですが、回を重ねるうちに、練習回数も増えて、自分が上手になっていくのが明らかにわかりました。
遺伝研で広がる研究


遺伝研には2021年10月に着任し、2023年度まではオーフス大学と兼任しています。日本でもいくつか助成金を得られたこともあって、2台の二光子顕微鏡を新しく購入することができました。遺伝研で行いたいと考えていることの1つは、霊長類を用いた解析です。マーモセットを用いた研究に着手して、マウスで見つけた知見がどれくらい霊長類とも共通しているか、あるいはどこが違うか、それを調べたいと思っています。そしてそれをヒトの視覚の理解や病気の治療にも役立つ知見に結びつけていきたいと考えています。
また、私の研究ではマウスを用いるのですが、遺伝研にはマウスの大規模な飼育施設があります。素晴らしい飼育環境に加えて、世界中のマウス亜種のコレクションが揃っているという特徴もあります。私は、これらのマウスを用いて、視覚と環境適応のメカニズムの研究も始めたいと考えています。どういうことかというと、マウスにはタカやフクロウといった天敵が上空を飛んでいるのを見ると逃げるという習性があります。黒い丸い用紙をマウスの上から見せると、マウスがシェルターに逃げ込むことが実験で確認されています。この反応には、マウスの亜種ごとの生息環境の違いがどう影響しているのか、天敵に違いはあるのか、鳥の形との関係はどうか、といったことを遺伝子のレベルから調べたいと思っています。網膜から、より高次のレベルの視覚システムの研究になると期待しています。


私が学生さんに望むことは、そうですね。何が面白いかまだわかってなくてもいいので、高いレベルで何かをやり遂げたいという意欲がある人、成長することを楽しいと思う人に来てほしいです。コミュニケーションがきちんととれる人でもあってほしい。ポスドクならば、自分が何をやりたいか、はっきりと分かっている人がよいですね。
私の若い頃は、日本の研究室で鍛えられたこともあり、休みなく働くハードワーカーでした。ロスカ研究室でも当初は無茶苦茶ハードワークを続けていましたが、体調を崩した時期がありました。それで、健康が何よりも大事だと改めて気づき、それからは、家族と過ごす時間や休暇をとって旅行する時間なども大切にするようにしています。周囲のヨーロッパの人たちを見回すと、華々しい業績を挙げている人たちでも、みな研究を楽しむ余裕をもっていることにとても驚きました。私の研究室も、楽しく研究できることを大切にしていきたいと思っています。そして、私が取り組んできた網膜の神経回路の研究を引き継ぎ、発展させてくれたら最高です。
聞き手:サイエンスライター 藤川 良子
写真撮影:遺伝研ORD 来栖 光彦
2022年8月
引用論文等
- *1 Expression of SPIG1 reveals development of a retinal ganglion cell subtype projecting to the medial terminal nucleus in the mouse
PLoS One. 2008 Feb 6;3(2):e1533. - *2 Identification of retinal ganglion cells and their projections involved in central transmission of information about upward and downward image motion
PLoS One. 2009 Jan 29;4(1):e4320. - *3 Spatially asymmetric reorganization of inhibition establishes a motion-sensitive circuit
Nature. 2011 Jan 20;469(7330):407-410. - *4 Congenital Nystagmus Gene FRMD7 Is Necessary for Establishing a Neuronal Circuit Asymmetry for Direction Selectivity
Neuron. 2016 Jan 6;89(1):177-93. - *5 Spatiotemporally Asymmetric Excitation Supports Mammalian Retinal Motion Sensitivity
Curr Biol. 2019 Oct 7;29(19):3277-3288. - *6 Direction selectivity in retinal bipolar cell axon terminals
Neuron. 2021 Sep 15;109(18):2928-2942.e8.. - *7 A segregated cortical stream for retinal direction selectivity
Nat Commun. 2020 Feb 11;11(1):831.
