


村山泰斗准教授は、生物の細胞の中で起こる生命現象を、細胞の外で再現する「試験管内再構成」の第一人者だ。細胞から精製したタンパク質を、試験管内で順序よく反応させ、「細胞の中身」を組み立て直す作業を通じて、あらためて細胞とは何かについて迫っていく。村山准教授が特に着目するのは、姉妹染色分体の形成と分配のしくみだ。2024年1月に、国際科学雑誌Natureに掲載された最新の成果を、背景や展望に触れながら紹介する。
村山 泰斗 [むらやま やすと]
日本大学生物資源科学科卒。横浜市立大学大学院国際総合科学研究科 博士課程修了。博士(理学)。2010年 英国がん研究基金研究所(現フランシス・クリック研究所)ポスドク研究員。東京工業大学助教を経て、2017年 国立遺伝学研究所 新分野創造センター 特任准教授、2022年 国立遺伝学研究所 遺伝メカニズム研究系 染色体生化学研究室 准教授。日本遺伝学会奨励賞、文部科学大臣表彰若手科学賞など受賞。
「姉妹染色分体間接着」という重要なしくみ


生物の細胞の中で起こる多様な化学反応は、生命活動そのものと言っても過言ではありません。詳細が明らかになっていないことも多く、個々の現象のメカニズムを解き明かす研究活動は、未だ試行錯誤の段階です。私たちは、複雑に絡み合う背景をできるだけ取り除きながら、細胞内で起こる一つひとつの現象を、試験管の中で再現するという手法を通して、生命のしくみを探究しています。
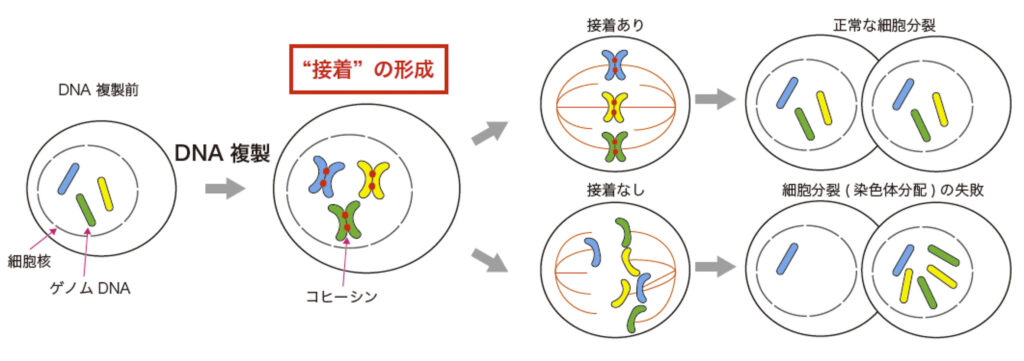
中でも私たちは、ヒトを含む真核生物の細胞が分裂して、増殖する為に不可欠な「姉妹染色分体間接着」という構造体に着目しています(図1)。私たち生命の設計図であるDNAは、細胞よりもはるかに長大な糸状の分子ポリマーです。例えばヒトの体細胞は、直径約20マイクロメートルとごく小さいにも関わらず、そのゲノムDNAは、全長約2メートルもの長さに及びます。細胞は、生命を維持するために分裂を繰り返して、絶えず新しい細胞を作り出します。分裂に先駆けて複製されたゲノムDNAは、分裂期に入ると凝集して、染色体と呼ばれるコンパクトな構造体になります。この時、複製されて2本になった染色体のペア(姉妹染色分体)には、物理的に接着する部位が生じます。この接着部位が「姉妹染色分体の間の接着」であり、分裂して新たにできる娘細胞へ、染色体を均等に分配するために不可欠な構造なのです。
染色体を分配するために、何故、わざわざ複製した2本の染色体を接着させる必要があるのでしょうか。分裂期の細胞の中では、紡錘体というラグビーボールのような構造ができますが、これが染色体を2つの娘細胞へと均等に運搬します。紡錘体の“手”にあたる微小菅が、細胞の両端から伸びてきて、染色体ペアをそれぞれ逆方向から掴みます。この時、姉妹染色体は接着しているので、紡錘体がそれぞれの方向に染色体を引っ張ろうとすると張力が生じます。この張力は、紡錘体がそれぞれの姉妹染色分体を正しく掴んで、正しい方向に引っ張っているという重要な合図となります。この状態になってから接着が取り除かれることで、娘細胞に正確に染色体を受け渡すことができるのです。接着がなければ、紡錘体は染色体をランダムに掴んでしまうため、均等な分配が行われなくなり、細胞は死滅してしまいます(図1)。
このように、非常に重要な役割を果たす姉妹染色分体間接着ですが、接着を形成・維持するシステムに異常が生じるということもあります。そうなると、染色体の分配エラーが起こり、染色体の構造異常や異数化につながります。そして、このような異常は、細胞のガン化などと密接に関連しているようです。また、生殖細胞を作る際の減数分裂においても、染色体間の接着が、配偶子の形成に不可欠であることも見えてきました。染色体間に形成される接着を制御するメカニズムの解明は、さまざまな疾病や不妊などが生じる原因の究明につながる可能性があります。

人工的に再現することで分かってきた接着の形成メカニズム
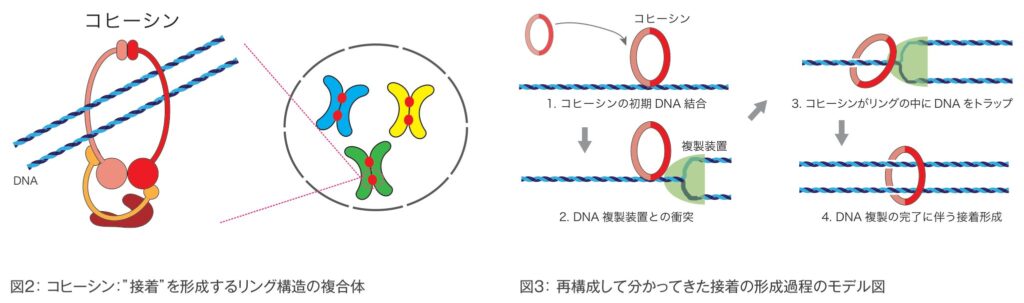
先にも触れましたが、生物のゲノムDNAは、細胞よりもはるかに長大です。細胞の中には、この長いゲノムDNAに結合し、折りたたんでまとめる役割を持つタンパク質が多数存在しています。姉妹染色分体間接着を形成するのも、「コヒーシン」と呼ばれるDNAに作用するタンパク質複合体の一種です。DNAに結合するタンパク質は、ヒストンをはじめ、さまざまな種類がありますが、その中でもコヒーシンは、リング状の構造を持った特徴的な形をしています。コヒーシンは、四半世紀近く前に同定され、このリング構造を利用して、接着を形成すると長らく考えられてきました。つまりコヒーシンは、姉妹染色分体の一対のDNAをリングの中に取り込み、束ねる分子バンドルとして働くことで、接着を形成するであろうというモデルです(図2)。絵にすると非常に分かりやすく合理的です。しかし、その分子メカニズムは、未だ明らかにされていません。私たちは目下、こ人工的に再現することで分かってきた接着の形成メカニズムの重要なタンパク質の働きの全容解明に挑んでいます。
2024年の1月には、成果の一つを「Coordination of cohesin and DNA replication observed with purified proteins」と題した論文にまとめ、国際科学雑誌Natureで発表することができました(*1)。コヒーシンによる、接着形成の分子メカニズムの解明に迫るものです。
明らかになった接着形成のイメージは、次の通りです(図3)。まずコヒーシンが、DNAに結合します。次に、コヒーシンが結合しているDNA上に、複数のタンパク質から構成されるDNA複製装置が形成されます。その後、この複製装置はDNA合成を伴いながら進行し、コヒーシンと衝突します。この衝突の時に、コヒーシンのリング構造の一部が開き、リングの中にDNAが取り込まれます。この状態で複製が完了することにより、複製装置によって作られた2本の“姉妹”DNAがコヒーシンリングによって束ねられ、接着するというものです。本成果により、コヒーシンが複製された2本のDNA、つまり姉妹染色分体を接着する機構の全体像が見えてきたことになります。私たちはこれを、「試験管内再構成」を成功させることで明らかにしました。
試験管内再構成とは、細胞から必要なタンパク質を集め、試験管の中で順序よく反応させていき、細胞内で起こる現象を再現することです。細胞内では、様々な生命反応が同時進行しており、染色体に関わるタンパク質だけでも、1000種類以上が存在します。接着の形成メカニズムに迫るためには、複雑性をなるべく排除し、一つひとつの反応を取り出して調べていく、本手法が強みになりました。

試行錯誤を繰り返す、肝となる2つのステップ
試験管内再構成には、大きく分けると2つの段階があります。第一に、材料となるタンパク質を細胞から精製すること、そして第二に、そのタンパク質を細胞の外で起動させ、そのタンパク質がもつ固有の生化学活性を、試験管の中で引き出すための実験条件を見つけることです。
まずは、細胞から再構成に必要なタンパク質を取り出し、精製します。その際、実験に必要な量を得るために、目的とするタンパク質を大量に発現させる細胞株を構築しなければなりません。タンパク質によっては、こうした精製法の確立に数週間を要するものから、年単位がかかる厄介なものまで千差万別です。残念なことに、コヒーシンは後者でした。まず、代表的なタンパク質発現システムである、大腸菌系や昆虫細胞系での精製を試しましたが、いずれもうまくいきませんでした。コヒーシンは、4つのサブユニットが集まって組み上がるタンパク質複合体の一種ですが、一見精製できたように見えても、サブユニットの割合がおかしいものが採れてしまうなど、失敗が続きました。各サブユニットを別々に精製して、再度組み立て直すという方法もありますが、それも困難なことが分かりました。こうした既存の方法を、色々と試していきましたが、再構成に足るコヒーシンの精製は叶わず、次の手と言っても、当時は候補となる細胞がない状態でした。後は、さまざまな細胞でひたすら試していくしかなく、ようやく現在用いている出芽酵母に辿り着きました。この間、およそ2年にわたる試行錯誤となりました。このように試験管内再構成では、必要なタンパク質を、一つずつ単独で精製する実験系を整えることから始めなくてはならず、非常に根気の必要なものになるケースも少なくありません。
精製法が確立できた後は、目的とするタンパク質の活性を、試験管の中で再現する作業になります。過去報告された研究を足がかりに、目的とするタンパク質が持ち得る活性を想定し、それが検出可能な実験をデザインします。コヒーシンの場合、姉妹染色分体間接着を形成するために必要な活性として、1)コヒーシンのリング構造の中にDNAを取り込む特殊なDNA結合、そして、2)コヒーシンがATPアーゼの一種であることから、ATPを入れた時のみ、このDNA結合反応が起こる、ということが想定されます。この仮説を満たす反応が、コヒーシンによって起こるか否かを検証していきます。試験管内再構成は、通常10~20マイクロリットルの反応液中で行いますが、この中にコヒーシン、DNA、ATPを加えます。さらに、pHを安定させるバッファーや、ATPアーゼの活性に必要なマグネシウムイオンなど、コヒーシンの活性を試験管内再構成するために、最低限必要と考えられる物質を添加していきます。この時、添加する物質の種類だけでなく、濃度等の微調整も肝要となります。本来は、細胞の中で最適に働くタンパク質を、細胞の外で扱うことから、本来の活性を引き出す条件を整えるためには、時間と経験を費やす検討が必要になります。わずかな条件のゆらぎが、タンパク質の活性に影響を与えることも多いため、ここは一つひとつ根気強く取り組む必要があるのです。そしてこれらの条件は、同じコヒーシンを対象とする実験であっても、どのような反応を再構成するのかによって変わっていきます。





再構成だからこそ明らかにできるもの
コヒーシンを精製し、再構成の条件を見定めながら、私たちはまず、コヒーシンがDNAをリング構造の中に取り
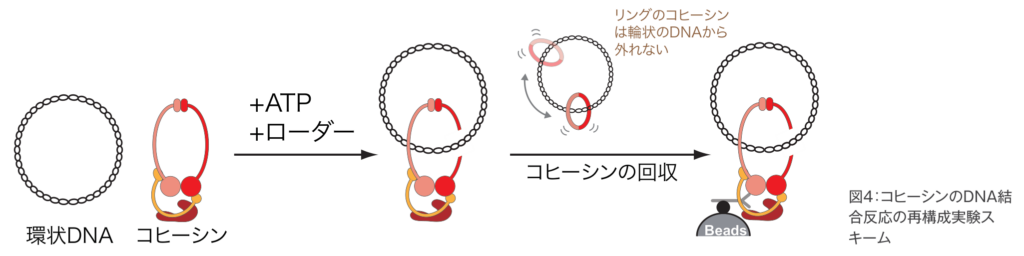
込むという活性を、本当に有するのかどうかを検証していきました。ところで、どうやって“リングの中にDNAが通っている”という状態を検出したらいいでしょうか。電子顕微鏡などで観察するというのは、最も直接的です。しかし、こういった方法は非常に時間がかかるため、この活性が本当にあるかどうかも分からないまま、反応条件を設定し、実験を行うというのは現実的ではありません。また、後に他グループの研究から、コヒーシンは柔らかくフレキシブルなリング構造を作るため、たとえ電子顕微鏡で見たとしても、リング形を観察できるものは少ないことも分かってきました。そこで、簡便で迅速に活性を検出できるように、次のような実験をデザインしました(図4)。
コヒーシンと短い輪状のDNAを用いた実験です。コヒーシンが、DNA鎖をリングの中に捕縛した場合、リング状のコヒーシンの中に、リング状のDNAが通ることになるため、輪状DNAは、そう簡単にはコヒーシンから外れないはずです。逆に、この輪状DNAを一箇所で切断して線状にすると、コヒーシンはDNAの末端からするりと落ちて、結果的にDNAと結合しなくなるはずです。この反応が起こることを期待しながら、実験チューブの中にATPを入れた状態で、コヒーシンと輪状DNAを加え、しばらく放置します。その後、免疫沈降という方法でコヒーシンを回収します。そうすると、コヒーシンがDNAと結合していた場合、このDNAも一緒に回収されるだろうという寸法です。細かいことですが、この免疫沈降で回収する時、高塩濃度のバッファーで処理しました。一般的にDNA結合タンパク質の多くは、高塩濃度になるとDNAから外れる傾向にありますが、このような処理を経ても、コヒーシンと一緒にDNAが回収されれば、コヒーシンがリング構造の中にDNAを捕縛し、簡単には外れない構造になっている証拠の一つになります。このDNAを、学生実験でもよく使われるゲル電気泳動で検出しました(図5)。この方法ならば、実験開始から検出まで、一日で終わらせることができるため、反応条件の検討も早いサイクルで行えると考えました。
いくつかの条件を検討しましたが、結果は芳しくありませんでした。ATP依存的にコヒーシンによって輪状DNAが回収されるものの、その活性があまりにも低かったからです。これは、ある意味では予想通りの結果で、細胞を調べた文献をあたると、コヒーシンがゲノムDNAに結合し、接着を形成する為には、コヒーシン以外のタンパク質が機能していることが散見されます。その中で最も有力なのは、ローダーと呼ばれるタンパク質複合体です。しかしローダーが、コヒーシンを直接活性化すると証明する実験は、過去に例がありませんでした。そこで私たちは、ローダーを加えた状態で試行錯誤を繰り返し、コヒーシンはATPとローダー存在下で、効率的かつ安定的に輪状DNAと結合することを突き止めました。その後、一連の検証実験を行い、コヒーシンがリング構造の中にDNAを通す活性を確かに有するとともに、それが細胞で見られる必須要素(ATPとローダー)に依存して起こるということを、試験管内で再現し、証明しました。これは、コヒーシンがDNAに結合するためには、ローダーが必要であることを明らかにした、世界でも初めての成果になりました(*2)。さまざまな生命反応が複雑に絡み合う細胞内では、確認が困難な仮説を、試験管内再構成で立証できた一例となります。この実験系をうまく応用して研究を進めていった結果、コヒーシンのDNAに結合する活性が、どのように制御されているかが段々と、そして詳細に分かっていきました(*3,*4,*5)。
「接着形成」という一つの細胞内経路の再現に挑戦
コヒーシンが、姉妹染色分体間接着を形成するのに必要な、DNA結合活性を持っていることは分かりました。では、姉妹染色分体間接着は、いつ、どのようにして出来上がるのでしょうか。いつ、については明確に分かっています。酵母を用いて遺伝学的なトリックを駆使した研究で、コヒーシンがない状態でDNA複製を終わらせ、その後G2期(分裂準備期)にコヒーシンを発現させた、というものがあります。一対の姉妹染色分体ができている状態で、その後からコヒーシンを発現させたことになるのですが、この場合、コヒーシンがあるにも関わらず、接着が形成されません。このことは、姉妹染色分体間接着は、DNA複製が起こっている最中に形成されることを強く示唆しています。実際に、DNA複製を行うタンパク質超複合体(複製装置)に結合する因子のいくつかが、接着の形成に機能することも報告されていました。この背景から、接着の形成機構を知るためには、コヒーシンとDNA複製の関わりを調べる必要があり、この過程を再構成することで検証できないかと考えていました。
複製装置を形成させ、DNA複製を再構成する為には、DNAの2本鎖を開裂させるヘリカーゼや、DNAを合成するポリメラーゼなど、さまざまなタンパク質が必要であり、その数は20種類以上に及びます。前述のように、コヒーシンの精製法の確立に、2年間を費やすことになったため、これは大変な工程になるだろうと予測していました。しかし幸いなことに、DNA複製研究の大家で、本所の荒木弘之名誉教授のご厚意で、複製に必要なタンパク質のセットを引き継ぐことができました。これは本当に幸運なことで、さらに不足したタンパク質因子を精製する必要はありましたが、予想よりもはるかにスピーディーに研究を進めることができました。
そして、今回の試験管内再構成でも、反応条件の微調整に時間を要しました。塩濃度のわずかな差異で反応が進まなくなることが分かり、濃度をごくわずかに変えては実験するということを、ひたすら繰り返していきました。余談になりますが、精製したタンパク質を試験管内で扱おうとすると、試験管壁に付着するなどして、うまく機能しないということもあります。対処するために、適切なブロッキング材を選択するなど、試験管内再構成に特有のハードルにも対応しながら、実験を進めていく必要があります。
コヒーシンが活性を示し、DNAの複製が進みやすい試験管内の環境を整えながら、必要なタンパク質を順序よく混ぜていくことで、再構成を進めていきました。その上で、コヒーシンが複製されたDNAと結合しているか否か、結合した場合は、どのような複製状態であるかを、ゲル電気泳動で確認していきます。コヒーシンと複製の完了した一対のDNAが、結合を維持した状態で検出できれば、複製の進行に伴い、コヒーシンがそれらを束ねるように働いたことの指標になります。これらの実験を繰り返し、さまざまな補助実験も実施して証拠を集め、反応の機序を組み立てていきました。冒頭で示した接着の形成過程は、こうして導き出したものです。
このように私たちは、精製したタンパク質を用いた実験で得られるデータから、細胞の中で起こる現象のメカニズムを、理論的に紐解いていくアプローチで研究を行っています。得られる実験データは、ゲル電気泳動で検出されるDNAを指標にするため、反応の過程を直接目で見て確認している訳ではありません。ある意味、間接的に検出しているわけですが、ゲル電気泳動のデータは非常にクリアです。条件をさまざまに変えながら解析を繰り返すことによって、見えない過程のロジックが、パズルのように組み上がっていきます。このデータを解釈する過程が、とても面白いところだと感じています。最終的には、一つひとつの反応が起こる様を、高解像度イメージングによって、経時的に追う実験法も構築したいと考えています。現在確立している間接的な実験系を元に発展させる形で、反応過程の状態をも明らかにできるような実験系を、組み立てていきたいと思います。
まだ研究者になることなど想像もしていなかった学部生の頃から、生物学の実習で扱う実験のプロトコールには、異常なほど興味を持っていたという思い出があります。複雑な実験系を整えることが肝となる研究手法は、今のところ私には、一番向いているアプローチであると実感しており、ぜひ続けて行きたいと考えています。


研究者として在り続けるために


私が、こうした分子生物学の分野に、関心を持ったきっかけを振り返れば、学部生の頃、核酸やDNA、タンパク質の働きなどを担当されていた先生の授業まで遡ります。当時PCで授業を行う先生の少なかった時期に、パワーポイントをいち早く取り入れ、途中で考えさせる質問を投げかけるような先生で、色々と面白く感じたのです。その後、修士課程、博士課程へと進む中で、DNAの相同組換えを対象とする研究を始めましたが、研究者になることは、当時はあまり意識していませんでした。しかし、実験データをロジカルに解釈し、それを組み立てて論文にまとめていく過程で、確かな面白さと手応えを感じました。
国内での博士研究員を経て、日本学術振興会の海外特別研究員制度も利用し、英国がん研究基金研究所(Cancer Research UK)へ赴いたのが、博士課程を修了した2年後のことでした。コヒーシンというテーマと出逢ったのは、この時になります。当時、コヒーシンの属するSMCタンパク質が、染色体の3次元構造の形成を制御するキーファクターであることは広く知られ、染色体研究分野でも注目因子でしたが、その生化学的な活性は明らかにされていませんでした。そのように重要とされるタンパク質が、どうやって働くのかを、誰もまだ再構成したことがないと言うなら、ぜひそれをやってみたいと考えたのです。実際に、採用の決め手となったのも、私がDNAの相同組換えや、修復反応を再構成する経験を有していたからだと思います。英国での4年半の研究を経て、日本へ帰国した後も、コヒーシンとその染色体接着機構が主要な研究テーマとなりました。
そして、私の最終的な関心は、どこまで頑張れば、細胞、そして生物を組み立てることができるのか、というところにあります。大きなことを言い過ぎるように聞こえるかも知れませんが、今回の試験管内再構成では、約30種類にも及ぶタンパク質を利用し、有機的に働かせるということを実現しました。これをどんどんボトムアップさせて、姉妹染色分体間接着や、染色体そのものの再構成というところまでは、ぜひ実現させていきたいと思っています。その先に、細胞や生物の再構成への展望が拓けて行くことを信じ、身に付けてきた手法を強みに、根気強く挑んでいきます。
聞き手:ノンフィクションライター 西岡 真由美
写真撮影:遺伝研ORD 来栖 光彦
デザイン:遺伝研ORD 澁谷 奈穂
2024年4月
引用論文等
- *1 Coordination of cohesin and DNA replication observed with purified proteins Nature.
2024 Feb ;626(7999):653-660 - *2 Biochemical reconstitution of topological DNA binding by the cohesin ring Nature. 2014
Jan 16;505(7483):367-371. - *3 DNA entry into and exit out of the cohesin ring by an interlocking gate mechanism
Cell. 2015 Dec 17;163(7):1628-1640. - *4 Establishment of DNA-DNA interactions by the cohesin ring
Cell. 2018 Jan 25;172(3):465-477. (*corresponding author) - *5 DNA binding by the Mis4Scc2 loader promotes topological DNA entrapment by the cohesin ring
Cell Rep. 2020 Nov 10;33(6):108357. (*corresponding author)
